カポジ肉腫関連ヘルペスウイルス(KSHV: Kaposi sarcoma–associated herpesvirus)は、カポジ肉腫の原因ウイルスとして知られるほか、敗血症様の臨床像を呈することがある。特に、固体臓器移植では、免疫抑制状態を背景として重篤化し、致死的経過をとることがある。しかし、ドナーに対するKSHVのルーチン検査は現在のところ確立されていない。CDCの週報(MMWR)に詳細が記述されているので、紹介する1)。
KSHV感染の背景と臨床的重要性
- KSHVは、ヒトヘルペスウイルス8型(HHV-8)としても知られ、カポジ肉腫(KS: Kaposi sarcoma)、多中心性キャッスルマン病(multicentric Castleman disease)、原発性滲出液リンパ腫(primary effusion lymphoma)といった特定のリンパ増殖性疾患の原因となるウイルスである。
- 近年、KSHV感染者に敗血症に類似した重篤な炎症症状を引き起こす「カポジ肉腫関連炎症性サイトカイン症候群(KICS: Kaposi sarcoma–associated inflammatory cytokine syndrome)」という病態が新たに報告されており、臨床現場での注意を要する。
- 固体臓器移植レシピエントは、移植片拒絶反応を防止するために免疫抑制剤を使用しているため、KSHV感染が重症化しやすく、致死的な経過をたどるリスクが高い。
- 移植後のKSHV関連合併症は、主に「潜伏感染の再活性化」、「移植後の新規感染」、および「移植臓器を介したドナー由来のウイルス伝播」の3つの経路によって発生する。
- 現在、米国においてはドナーおよびレシピエントに対するKSHVのルーチン検査は義務付けられておらず、商用検査キットの利用可能性が限られていることや、スクリーニングのガイドラインが確立されていないことが課題となっている。
- 本稿では、2021年1月から2025年9月にかけてCDCが調査した、ドナー由来と疑われるKSHV感染事例の急増と、その臨床的特徴について要旨をまとめる。
疫学的動向:ドナー由来感染報告の急増
- 2021年1月から2025年9月の期間、米国ではKSHVを伝播させた疑いのある死亡ドナーが46人特定された。
- これは、直前の5年間(2016〜2020年)に報告された9人と比較して、約5倍(500%)という顕著な増加を示している。実際、2010年から2020年までは年間数件にとどまっていた報告数が、2021年以降急激に上昇した(図1)。
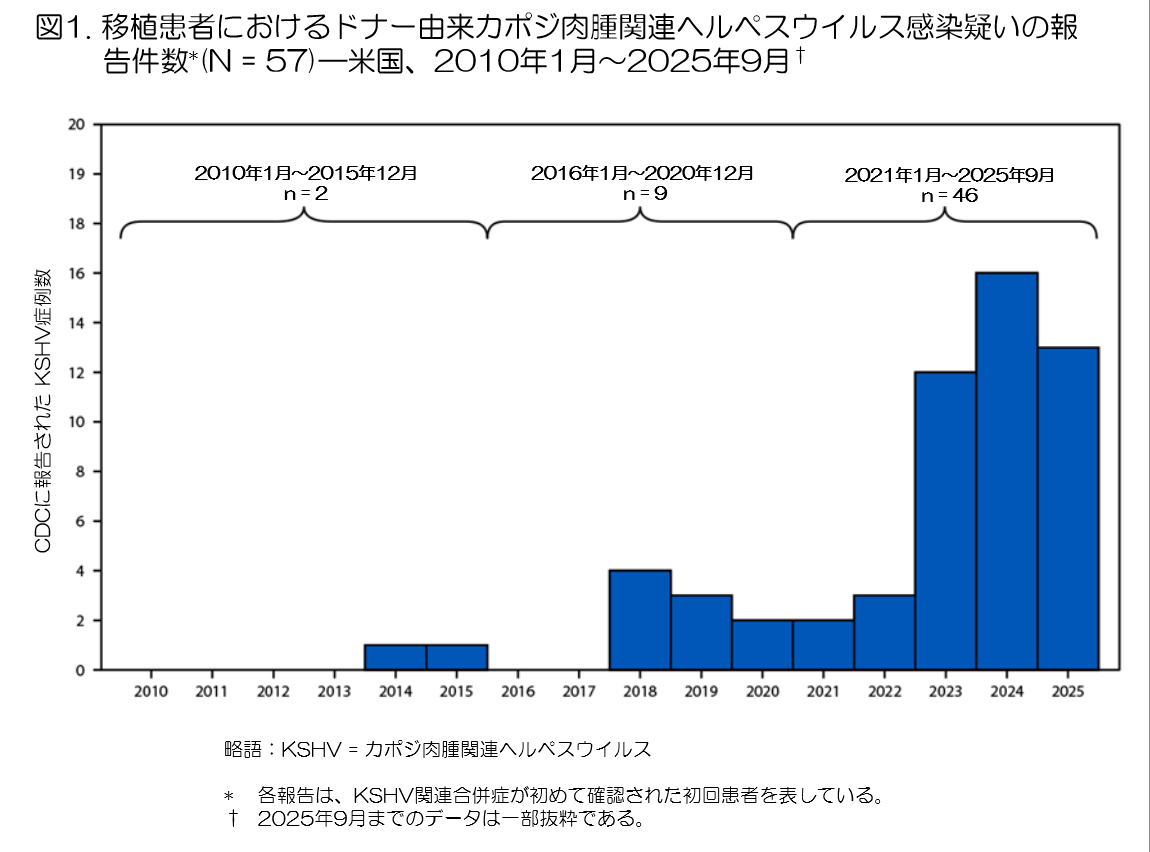
- この急増の背景には、臨床医の意識向上や報告体制の整備だけでなく、ドナー側のリスク因子の変化が関与している可能性が示唆されている。
ドナーおよびレシピエントの特性とリスク因子
- 歴史的に米国におけるKSHV伝播は、男性間性交渉者(MSM: men who have sex with men)やHIV感染者に関連することが多かったが、本調査の事例ではドナーおよびレシピエントの多くがHIV陰性であり、MSMでもなかった。
- 調査対象となった46人のドナーの年齢中央値は38.5歳であり、そのうち67%(31人)に非医療目的の吸入薬物または注射薬物の使用歴が認められた。具体的には、メタンフェタミン、コカイン、マリファナ、またはアルキルナイトレート(亜硝酸エステル)の吸入使用などが含まれる。
- 米国における全死亡ドナーのうち、急性薬物中毒を死因とする割合は、2010年の4%から2023年には17%へと上昇しており、オピオイドの流行がドナーのリスクプロファイルに影響を与えていると考えられる。
- 一方、レシピエント153人の年齢中央値は58.5歳であり、98%がHIV陰性であった。
移植後の感染状況と臨床的合併症
- 特定された46人のドナーから提供された185の臓器は、計153人のレシピエントに移植された。
- 最初に報告された46人の「インデックス・レシピエント」に加え、CDCの調査によってさらに28人の感染レシピエントが特定され、最終的に計74人(48%)のレシピエントで移植後のKSHV感染が確認された(図2)。また、このチャートには、未検査または評価中の55人についても示されている。
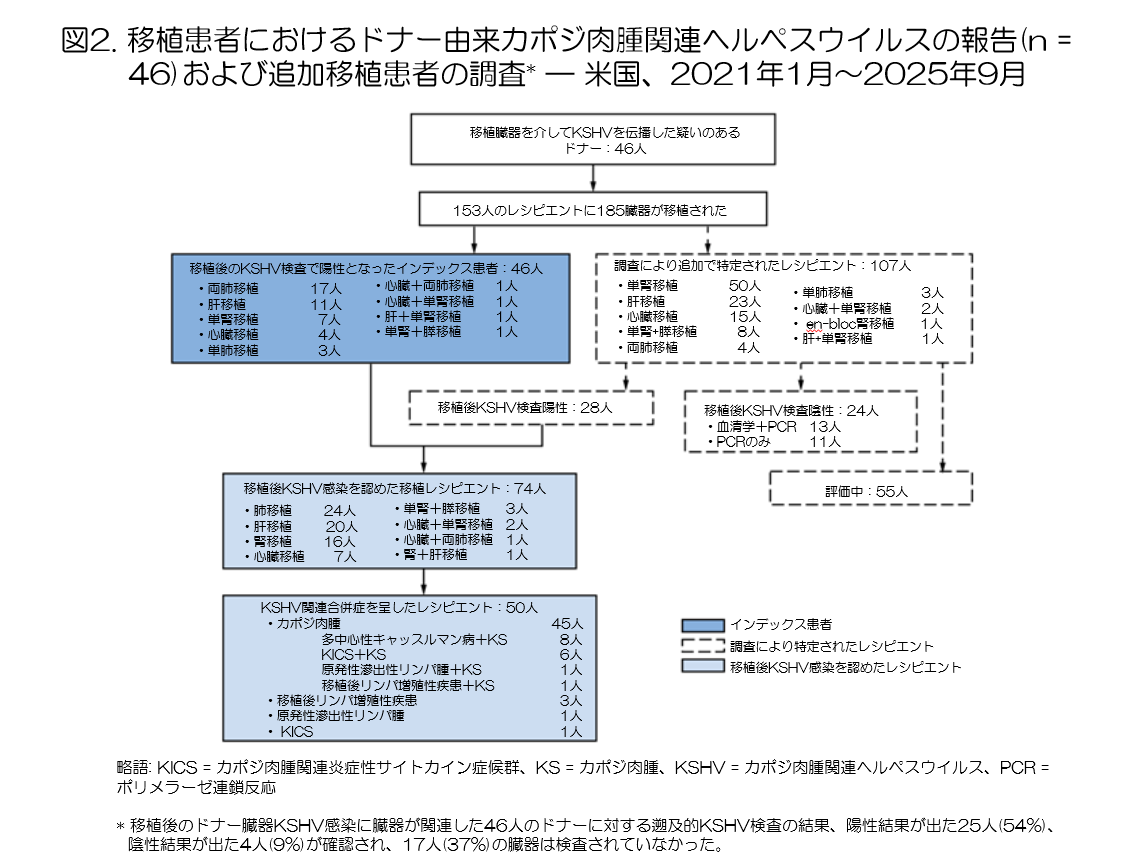
- 移植された臓器別のKSHV陽性率(レシピエント側)は、肺が86%(24/28人)と最も高く、次いで肝臓57%(20/35人)、心臓30%(7/23人)、腎臓22%(16/72人)であった(表)。移植から臨床症状の発現までの期間の中央値は208日であった。

- KSHV感染が確認された74人のうち、61%(45人)がカポジ肉腫(KS)を発症した。さらに、KSを発症した45人のうち、8人が多中心性キャッスルマン病、6人がKICS、2人が移植後リンパ増殖性疾患を併発していた。
- 4人(5%)はリンパ増殖性疾患のみ(原発性滲出液リンパ腫[1人]、移植後リンパ増殖性疾患[3人] )を発症し、1人(1%)はKICSのみを発症した。
- 2026年2月時点の集計では、153人のレシピエントのうち16%にあたる25人が死亡している。ただし、死因に対するKSHV感染の直接的な寄与については現在も調査中である。
診断および感染制御における課題
- KSHVの検査、特に血清学的検査の商用利用が限られていることが、ドナー由来感染の監視と追跡を困難にしている。
- 分子標的検査(PCR等)は血液中のウイルスDNAを常に検出できるわけではなく、偽陰性の可能性があるため、可能であれば血清学的検査と分子標的検査の両方を併用することが推奨される。
- KICSは症状が重症敗血症と酷似しているため、細菌培養が陰性の敗血症様症状を呈する移植レシピエントにおいては、KSHV関連の病態を鑑別診断に含めるべきである。
- ドナーが薬物使用などのリスク因子を有する場合や、同一ドナーから提供を受けた他のレシピエントの感染が判明した場合には、高い臨床的疑いを持って検査を実施する必要がある。
結論と提言
- 臓器移植によるKSHVのドナー由来伝播は、報告数が増加傾向にあり、移植後のレシピエントに深刻な合併症や死をもたらすリスクがある。
- しかし、臓器移植の利点は依然として感染リスクを上回っており、ドナー由来の疾患伝播の発生率は全移植レシピエントの0.5%未満であることも認識すべきである。
- 移植待機者の数は利用可能な臓器数をはるかに上回っており、感染症リスク因子を持つドナーからの臓器であっても、適切な管理の下で安全に使用できる可能性がある。
- 感染制御の専門家および臨床医は、移植臓器ネットワークへの迅速な報告を行い、ドナー・スクリーニング技術の向上とガイドラインの策定に協力することが、移植の安全性を高めるために求められる。
文献
- Kracalik I, et al. Kaposi Sarcoma–Associated Herpesvirus Infection and Complications Among Solid Organ Transplant Recipients — United States, January 2021–September 2025
https://www.cdc.gov/mmwr/volumes/75/wr/pdfs/mm7508a1-H.pdf
矢野 邦夫
浜松市感染症対策調整監
浜松医療センター感染症管理特別顧問








