消毒薬の選び方
消毒薬の調製上の留意点
1. 希釈に用いる水
水道水で希釈可能な消毒薬は、グルタラール(ステリゾールなど)、フタラール(ディスオーパ)、過酢酸(アセサイドなど)および次亜塩素酸ナトリウム(ピュリファンPなど)である。これらの消毒薬は抗菌スペクトルが広く、かつ殺菌力が強いので、少量の微生物(数個/mL)が含まれる水道水で希釈しても問題はなない1)。
一方、希釈して用いるポビドンヨード(イオダインMなど)は、粘膜や損傷皮膚への適用では滅菌精製水で希釈する。その他への適用では、水道水で希釈しても差し支えない。
また、クロルヘキシジン(ステリクロンなど)や塩化ベンザルコニウム(ザルコニンなど)を粘膜や損傷皮膚に用いる場合には、滅菌精製水で希釈するか、または精製水で希釈後に高圧蒸気滅菌を行う2)。ただし、希釈間違い防止の観点から、できる限り希釈・滅菌済み製品の使用が勧められる。なお、これらの消毒薬を手指や器具の消毒に用いる場合には、水道水で希釈する。この際には、水道水に少量含まれるセパシア菌(Burkholderia cepacia)などの細菌の高濃度増殖を防ぐため3-5)、希釈後24時間以内に廃棄する必要がある。希釈後24時間以上にわたって使用するのであれば、微生物汚染防止の目的で、1/10量のアルコールを添加しておくとよい6)。
両性界面活性剤(サテニジンなど)の希釈に用いる水は、クロルヘキシジンや塩化ベンザルコニウムの場合と同様である。
2. 希釈後の安定性(未使用の場合)
(1)グルタラール
緩衝化剤を添加後のグルタラール(ステリゾールなど)は、経時的に分解する。たとえば、蓋付き容器中の保管で、2%グルタラールの力価は14日後におおよそ50%となる7)。
(2)過酢酸
Ⅰ液とⅡ液を混合後の過酢酸(アセサイドなど)は経時的に分解する。たとえば、混合後9日間で約70%の力価となる。
(3)次亜塩素酸ナトリウム
希釈後の次亜塩素酸ナトリウム(ピュリファンPなど)は、遮光下での蓋付き容器中で1カ月間程度は安定である8,9)。ただし、本剤は有機物の混入で急速に力価低下が生じる。
(4)ポビドンヨード
希釈したポビドンヨード(イオダインMなど)は、密封・遮光保存では比較的安定で、1カ月間まで使用できる。しかし、洗面器などの開放容器中では不安定で、8~12時間で約半分の力価となる10)。
(5)クロルヘキシジン、塩化ベンザルコニウム、両性界面活性剤
希釈後のクロルヘキシジン(ステリクロンなど)、塩化ベンザルコニウム(ザルコニンなど)、両性界面活性剤(サテニジンなど)は安定である11,12)。希釈後に高圧蒸気滅菌しておけば、 密封・遮光保存で6カ月間は安定である。
3. 微生物汚染
表1には、高水準、中水準および低水準消毒薬の使用中の微生物汚染の有無について示した。
また、表2には、低水準消毒薬の典型的な細菌汚染パターンとその防止法を示した13-24)。
なお、自己導尿用カテーテルキット内への0.025%塩化ベンザルコニウム・グリセリン(グリセリンBC液60%「ケンエー」)の入れ替えは、微生物汚染防止の観点から、24時間ごとに行うのが望ましい25)。
表1. 使用中の消毒薬の微生物汚染の有無
| 分類 | 消毒薬 | 微生物汚染 | 備考 |
|---|---|---|---|
| 高水準 | グルタラール ステリゾールなど |
無 | |
| フタラール ディスオーパ |
|||
| 過酢酸 アセサイドなど |
|||
| 中水準 | 次亜塩素酸ナトリウム ピュリファンPなど |
無 | |
| ポビドンヨード イオダインMなど |
無 |
|
|
| アルコール 消毒用エタノールIPなど |
無 |
|
|
| 低水準 | 塩化ベンザルコニウム ザルコニンなど |
有 | |
| 塩化ベンゼトニウム ベゼトンなど |
|||
| クロルヘキシジン ステリクロンなど |
|||
| 両性界面活性剤 サテニジンなど |
|||
| アクリノール | 有 |
|
表2. 低水準消毒薬の微生物汚染パターンとその防止法
| 使用法 | 汚染パターン | 防止法 |
|---|---|---|
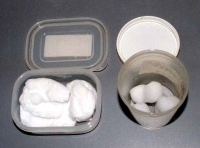 綿球やガーゼに含浸させて使用 |
長期間にわたる分割使用やつぎ足し使用 |
|
 気管内吸引チューブの浸漬に使用 |
24時間にわたるくり返し使用 |
|
 局所洗浄装置(イルリガートル)で使用 |
長期間にわたるつぎ足し使用 |
|
 バケツで使用 |
長期間にわたるつぎ足し使用 |
|
 ノズル式容器で使用 |
長期間にわたるつぎ足し使用 |
|
4. 使用開始後の使用期限
使用開始後の消毒薬の使用期限は、製品容器に記載されている年月までである。
一方、希釈または緩衝化して使用開始した消毒薬の使用期限は、使用方法、有機物汚染を受ける程度、気温、および日光照射の有無などの条件に左右される。表3には、使用開始後の消毒薬のおおよその使用期限と、その使用期限を左右する主な因子を示した。本表に関しての留意点は次のとおりである。
次亜塩素酸ナトリウム(ピュリファンPなど)では、目に見える有機物の混入が生じた場合はただちに作り換える必要がある8)。
希釈・滅菌済みのクロルヘキシジン(ステリクロンなど)や塩化ベンザルコニウム(ザルコニンなど)では、分割使用による微生物汚染は生じにくいので、開封後3カ月や6カ月にわたって分割使用できる14)。 ただし、容器注ぎ口やキャップの内側に手指などが触れた場合には、その時点での廃棄としたい。
表3. 消毒薬の使用開始後の使用期限
| 消毒薬 | 使用法 | 使用期間 | 使用期限を左右する因子 |
|---|---|---|---|
| グルタラール*1 ステリゾールなど |
内視鏡自動洗浄機 |
2~2.25%製品:20回もしくは7~10日間 3%製品:40回もしくは21~28日間 3.5%製品:50回もしくは28日間 |
|
| 浸漬容器 |
2~2.25%製品:7~10日間 3%製品:21~28日間 3.5%製品:28日間 |
||
| フタラール*2 ディスオーパ |
内視鏡自動洗浄機 | 30~40回 |
|
| 過酢酸*1,*3 アセサイドなど |
内視鏡自動洗浄機 | 25~30回もしくは7~9日間 |
|
| 浸漬容器 | 7~9日間 | ||
| 次亜塩素酸ナトリウム ピュリファンPなど |
浸漬容器 | 1~7日間 |
|
| ポビドンヨード イオダインMなど |
ベースン法 (洗面器など) |
8時間 |
|
| 消毒用エタノール | 万能つぼ | 7日間 |
|
| クロルヘキシジン ステリクロンなど 塩化ベンザルコニウム ザルコニンなど |
希釈・滅菌済み製剤の分割使用 | 3カ月間や6カ月間 |
|
| ベースン法 (洗面器など) |
8~24時間 |
|
- *1 グルタラールや過酢酸では、緩衝化剤を添加後の使用期限。
- *2 リンスが行いにくいという観点から、用手法(浸漬容器)での使用は勧められない。
- *3 金属腐食性が強いという観点から、浸漬時間は10分以内を厳守する。
5. 消毒薬綿球の使用期限
クロルヘキシジンや塩化ベンザルコニウムなどの低水準消毒薬を含浸した綿球(ガ―ゼ)は、細菌汚染を受けやすい13-16)。したがって、これらの低水準消毒薬の含浸綿球の調製後の使用期限は、24時間とする(表4)。
なお、低水準消毒薬の含浸綿球は細菌汚染を受ける可能性があるので、けっしてアンプルやバイアルの消毒に用いてはならない21,22,26) 。アルコール含浸綿球を用いる。アルコールは殺菌力が強く、かつ速乾性で、細菌汚染を受ける可能性がないからである(泥などの混入による芽胞汚染を除く)。
表4. 消毒薬の含浸綿球の使用期限(室温保管)
| 消毒薬 | 使用期限 |
|---|---|
| ポビドンヨード アルコール*1 |
7~14日間 |
| クロルヘキシジン 塩化ベンザルコニウム 塩化ベンゼトニウム 両性界面活性剤 アクリノール |
24時間 |
- *1 密封容器内では、より長期間使用できる。
引用文献
- Dukes MNG (ed.) : Side Effects of Drugs Annual 9, pp228-229,1985,Elsevier, Amsterdam
- Speller DCE, et al : Hospital infection by Pseudomonas cepacia, Lancet 1971; 1, 798-799.
- Bassett DCJ, et al : Wound infection with Pseudomonas multivorans : A water-bone contaminant of disinfectant solutions, Lancet 1971; l, 1188-1191.
- Burdon DW, Whitby JL: Contamination of hospital disinfectants with Pseudomonas species. Br Med J. 1967; 2, 153-155.
- Nakashima AK, et al : Survival of Serratia marcescens in benzalkonium chloride and in multipledose medication vials : Relationship to epidemic septic arthritis. J Clin Microbiol 1987; 25, 1019-1021.
- 尾家重治,神代 昭:クロルヘキシジンと低濃度エタノールとの併用による消毒効果,薬学雑誌 1984;104,780-785.
- Power EGM, Russell AD: Sporicidal action of alkaline glutaraldehyde: Factors influencing activity and a comparison with other aldehydes. J Appl Bacteriol 1990; 69, 261-268.
- Coates D: A comparison of sodium hypochlorite and sodium dichloroisocyanurate products. J Hosp Infect. 1985; 6, 31-40.
- Rutala WA, et al: Stability and bactericidal activity of chlorine solution. Infect Control Hosp Epidemiol 1998; 19, 323-327.
- 明治製菓・社内資料
- Gelinas P, Goulet J: Heat and light stability of eight sanitizers. J Food Protect 1982; 45,1195-1196.
- Goodall RR, et al: Stability of chlorhexidine solutions . Pharm J. 200:33-34,1968
- Oie S, Kamiya A: Microbial contamination of antiseptics and disinfectants. Am J Infect Control 1996; 24, 389-395.
- Oie S, Kamiya A: Microbial contamination of antiseptic-soaked cotton balls. Biol Pharm Bull 1997; 20, 667-669.
- Oie S, Kamiya A: Microbial contamination of water-soaked cotton gauze and its cause. Microbios 2001; 104, 159-166.
- Oie S, Kamiya A: Bacterial contamination of commercially available ethacridine lactate (acrinol) products. J Hosp Infect. 1996; 34, 51-58.
- 尾家重治,神谷 晃:気管内チューブの微生物汚染とその対策.日環感, 1993;8,15-18.
- 尾家重治,藤田陽子,石光 淳ほか:気管内チューブ浸漬用消毒薬の使用後の微生物汚染調査. 医学と薬学, 1999;42,989-991.
- McAllister TA, Lucas CE, Mocan H, et al:Serratia mercescens outbreak in a paediatric oncology unit traced to contaminated chlorhexidine.Scot Med J. 1989; 34, 525-528.
- Jumaa P, Chattopadhyay B:Outbreak of gentamicin, ciprofloxacin-resistant Pseudomonas aeruginosa in an intensive care unit,traced to contaminated quivers.J Hosp Infect. 1994; 28, 209-218.
- Olson RK, Voorhees RE, Eitzen HE, et al: Cluster of postinjection abscesses related to corticosteroid injections and use of benzalkonium chloride. West J Med 1999; 170, 143-147.
- Nakashima AK, McCarthy MA, Martone WJ et al: Epidemic septic arthritis caused by Serratia marcescens and associated with a benzalkonium chloride antiseptic. J Clin Microbiol 1987; 25, 1014-1018.
- Pegues DA, Arathoon EG, Samayoa B, et al: Epidemic gram-negative bacteremia in a neonatal intensive care unit in Guatemala. Am J Infect Control 1994; 22, 163-171.
- Bosi C, Davin-Regli A, Charrel R, et al: Serratia marcescens nosocomial outbreak due to contamination of hexidine solution. J Hosp Infect. 1996; 33, 217-222.
- Oie S, Kamiya A, Seto T, et al: Microbial contamination of in-use luburicants for non-touch urethral catheters in intermittent self-catheterization. Biol Pharm Bull 2000; 23,781-783.
- 西口裕,庄司正,寺井謙二,他:点滴を原因とするセラチア菌院内感染事例. Infect Agents Surveilance Report(国立感染症研究所), 2009; 30: 53-54.







